美國制藥巨頭禮來(Eli Lilly)近日宣布,啟動III期LIBRETTO-531臨床試驗(NCT04211337),評估口服RET激酶抑制劑selpercatinib(又名LOXO-292)一線治療RET突變甲狀腺髓樣癌(MTC)患者。這是評估selpercatinib的第二項III期研究,之前,禮來已啟動了首個III期LIBRETTO-431,評估selpercatinib一線治療RET融合陽性非小細胞肺癌(NSCLC)患者。
該研究將入組400例晚期或轉移性RET突變MTC患者,這些患者先前未接受過系統療法治療轉移性疾病。研究中,患者將以2:1的比例隨機分配接受2種方案(a、selpercatinib治療;b、醫生選擇的療法[cabozantinib或vandetanib])作為初始治療。RET突變將使用本地測試識別。研究的療效終點是無進展生存期(PFS)、無治療失敗生存期(TFFS)、總生存期(OS)、總緩解率(ORR)、緩解持續時間(DoR)。隨機分配至對照組的患者,在疾病進展時允許交叉。
今年9月底,禮來在2019 ESMO年會上公布了I/II期臨床研究LIBRETTO-001的數據。該研究是評估一種RET抑制劑治療RET改變癌癥患者的最大規模臨床研究。結果顯示,selpercatinib在先前未接受治療(初治)和先前已接受過治療(經治)的RET突變甲狀腺髓樣癌(MTC)患者中的ORR分別為59%和56%。之前公布的NSCLC隊列數據顯示,selpercatinib在初治、經治RET融合陽性NSCLC患者中的ORR分別為85%、68%;此外,selpercatinib是第一個顯示出強大中樞神經系統(CNS)活性的RET抑制劑,CNS ORR高達91%。
麻省總醫院癌癥中心、頭頸癌中心醫學主任Lori Wirth表示:“大約60%的MTC患者具有激活的RET點突變,但目前的治療方案對于許多患者來說并不理想。在晚期或轉移性RET突變MTC患者中開展的這項III期試驗,旨在確定新的治療標準。我們希望這將為這一患者群體提供更有效的治療選擇。”
美國甲狀腺癌患者協會 (ThyCa)執行董事Gary Bloom表示:“雖然MTC很少見,但在MTC中RET突變的發生率很高。因此,我們對這項III期試驗的啟動感到非常興奮,因為它將為晚期和轉移性RET突變MTC患者帶來希望。由于新的治療方案,MTC患者必須與他們的醫生討論是否以及何時應該對他們的腫瘤進行基因組檢測。這將確保有RET突變的患者有機會獲得潛在的治療以及參加臨床試驗,比如這一項針對selpercatinib的試驗。”
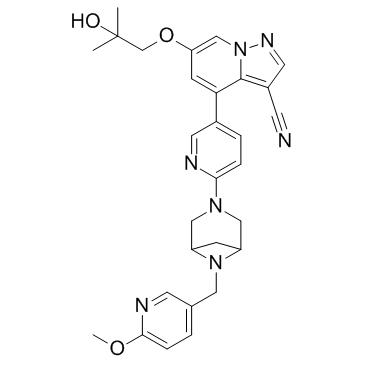
selpercatinib分子結構式(圖片來源medchemexpress.cn)
selpercatinib(LOXO-292)是一種強效、口服、高度選擇性轉染期間重排(RET)激酶抑制劑,用于治療RET異常的癌癥患者。RET基因是一個在轉染過程中發生重排的原癌基因,并因此而得名,該基因編碼一種細胞膜受體酪氨酸激酶,其異常是多種類型腫瘤的罕見驅動因素。據估計,RET融合存在于大約2%的非小細胞肺癌(NSCLC)、10-20%的乳頭狀甲狀腺癌(PTC)和其他類型甲狀腺癌、以及其他癌癥(如結直腸癌)亞組中;RET點突變存在于大約60%的甲狀腺髓樣癌(MTC)中。RET融合及RET點突變癌癥主要依賴于RET激酶的激活來維持其增殖和存活,這種依賴性通常被稱為“致癌基因成癮”,使得這類腫瘤對靶向RET的小分子抑制劑高度敏感。
selpercatinib旨在抑制天然的RET信號轉導以及預期的獲得性耐藥機制,該藥目前處于臨床開發,用于腫瘤中攜帶異常的RET激酶的患者。在美國監管方面,FDA已授予selpercatinib治療三類患者的突破性藥物資格(BTD),具體為:(1)接受含鉑化療以及一種PD-1或PD-L1腫瘤免疫療法治療后病情進展、需要系統治療(全身治療)的轉移性RET融合陽性NSCLC患者;(2)既往接受治療后病情進展且沒有可接受的替代治療選擇、需要系統治療的RET突變型甲狀腺髓樣癌(MTC)患者;(3)既往接受其他方案后病情進展且沒有可接受的替代治療方案、需要系統治療的晚期RET融合陽性甲狀腺癌患者。
selpercatinib由美國腫瘤學精準藥物開發公司Loxo Oncology發現,禮來在今年1月初以80億美元將其收購。除了selpercatinib之外,還獲得了Loxo公司多款靶向藥物,包括:(1)“廣譜”抗癌藥Vitrakvi(larotrectinib),與拜耳合作開發,這是一種原肌球蛋白受體激酶(TRK)抑制劑,已獲批用于治療NTRK基因融合陽性實體瘤;(2)LOXO-195,與拜耳合作開發,這是一種新一代TRK抑制劑,用于克服潛在的獲得性耐藥;(3)LOXO-305,這是一種可逆性BTK抑制劑,處于臨床前開發,治療B細胞癌;(4)FGFR項目,處于臨床前開發,治療成纖維細胞生長因子受體(FGFR)存在異常改變的癌癥。
近日,中國科學院合肥物質科學研究院健康與醫學技術研究所研究員劉青松、劉靜帶領的藥學團隊,開發出針對B細胞性非霍奇金淋巴瘤的新一代高選擇性、高活性BTK激酶抑制劑CHMFL-BTK-85。這是繼CHMF......
再鼎醫藥合作伙伴DecipheraPharmaceuticals是一家專注于解決腫瘤耐藥關鍵機制的臨床階段生物制藥公司。近日,Deciphera公司宣布,美國食品和藥物管理局(FDA)已受理廣譜KIT......
和黃中國醫藥科技有限公司(簡稱“和黃醫藥”或“Chi-Med”)近日宣布,在中國啟動了一項索凡替尼聯合拓益(特瑞普利單抗,首個國產PD-1單抗,君實生物研制)治療晚期實體瘤患者的II期臨床試驗。這是繼......
美國制藥巨頭禮來(EliLilly)近日宣布,啟動III期LIBRETTO-531臨床試驗(NCT04211337),評估口服RET激酶抑制劑selpercatinib(又名LOXO-292)一線治療......
美國制藥巨頭禮來(EliLilly)近日宣布,啟動III期LIBRETTO-531臨床試驗(NCT04211337),評估口服RET激酶抑制劑selpercatinib(又名LOXO-292)一線治療......
再鼎醫藥合作伙伴DecipheraPharmaceuticals是一家專注于解決腫瘤耐藥關鍵機制的臨床階段生物制藥公司。近日,Deciphera公司宣布,已向美國食品和藥物管理局(FDA)提交了廣譜K......
2019年國際肺癌研究協會(IASLC)主辦的第20屆世界肺癌大會(WCLC)于9月7-10日在西班牙巴塞羅那召開。此次會議上,禮來(EliLilly)公布了支持注冊口服RET激酶抑制劑selperc......
6月18日,百濟神州與SpringWorksTherapeutics,Inc.宣布成立MapKure,LLC,由雙方共同擁有。MapKure的創立旨在開發BGB-3245——一款針對特定單聚體和二聚體......
記者從中科院合肥物質科學研究院獲悉,該院強磁場科學中心劉青松研究員和劉靜研究員課題組在CDK家族激酶中研發出高選擇性的新型CDK9激酶抑制劑JSH-150,其有潛力成為廣譜抗腫瘤靶向藥物。研究成果日前......
近日,中國科學院合肥物質科學研究院強磁場科學中心研究員劉青松和劉靜課題組在CDK家族激酶中研發出高選擇性的新型CDK9激酶抑制劑JSH-150,其有潛力成為廣譜抗腫瘤靶向藥物。該研究成果在線發表在藥物......