Mesoblast Ltd是一家總部位于澳大利亞墨爾本的生物技術公司,是同種異體(通用型)細胞療法的全球領導者,致力于開發以細胞為基礎的再生治療產品,用于炎癥性疾病的治療。近日,該公司宣布,美國食品和藥物管理局(FDA)已受理其同種異體細胞療法Ryoncil(remestemcel-L)的生物制品許可申請(BLA)并授予了優先審查。Ryoncil是一種同種異體間充質干細胞(MSC)療法,用于治療類固醇難治性急性移植物抗宿主病(SR-aGVHD)兒童患者。FDA已指定該BLA的處方藥用戶收費法(PDUFA)目標日期為2020年9月30日。如果獲得批準,Mesoblast公司計劃將Ryoncil立即推向市場。此前,FDA已授予Ryoncil治療SR-aGVHD的快速通道資格(FTD)。
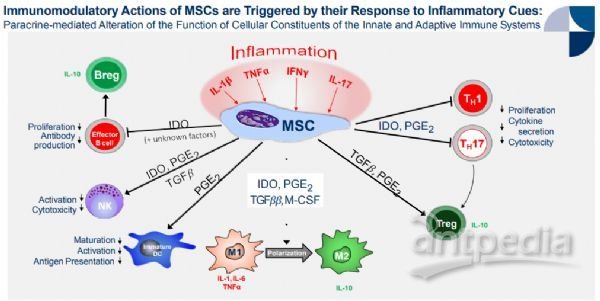
remestemcel-L是一種同種異體間充質干細胞(MSC),來源于不相關供體骨髓中分離的MSC并進行培養擴增制備而成。remestemcel-L通過靜脈輸注給藥,具有免疫調節作用,通過下調促炎細胞因子的產生、增加抗炎細胞因子的產生、并能將自然產生的抗炎細胞招募到相關組織中,來對抗與多種疾病相關的炎癥過程。
急性移植物抗宿主病(aGVHD)是一種潛在危機生命的疾病,發生在約50%的接受異基因骨髓移植(BMT)患者中。在全球范圍內,每年有超過3萬例患者接受異基因BMT,主要是在治療血液癌癥期間,20-25%是兒童。在aGVHD最嚴重類型(C/D級或III/IV級)的患者中,12個月死亡率高達90%。在美國,對于12歲以下SR-aGVHD兒童患者,目前尚無FDA批準的治療藥物。
Ryoncil的生物制品許可申請(BLA)中納入了多項臨床試驗。Ryoncil已在三項臨床研究中被用于治療309例SR-aGVHD兒童患者。在擴大獲取項目中,Ryoncil被用作挽救療法,治療了241例接受機構標準護理(類固醇和其他藥物)治療失敗的SR-aGVHD兒童患者。在開放標簽III期試驗中,Ryoncil還被用作一線療法治療了55例SR-aGVHD兒童患者,其中89%為C/D級疾病。
在BLA中,Mesoblast公司還納入了西奈山急性GVHD國際聯合會(MAGIC)同期數據庫中接受機構標準護理治療、與開放標簽III期入組標準和疾病嚴重程度相匹配的兒童對照組患者數據。開放標簽III期研究與MAGIC同期對照組的對比分析結果,支持了Ryoncil在SR-aGVHD兒童患者中的有效性,特別是在最嚴重的兒童患者中的有效性和生存獲益。這些結論得到了擴大獲取項目中241例兒童結果的支持。
具體數據為:開放標簽III期研究中,接受Ryoncil治療的55例SR-aGVHD兒童患者(89%患有C/D級疾病),第28天總緩解率為70%、第100天生存率為75%。這些結果優于來自MAGIC同期數據庫中相匹配的30例SR-aGVHD兒童患者的結果,在該對照組中,第28天總緩解率為43%、第100天生存率為57%。
目前,Ryoncil正在多項臨床試驗中,評估治療多種炎癥性疾病,包括SR-aGVHD(兒童、成人)、慢性GVHD、生物制劑難治性克羅恩病、缺氧缺血性腦病、大皰性表皮松解、老年肺部疾病患者。
Ryoncil通過靜脈注射給藥,目前正在多項臨床試驗中,評估治療多種炎癥性疾病,包括老年肺部疾病患者、成人和兒童SR-aGVHD、慢性GVHD、生物制劑難治性克羅恩病、缺氧缺血性腦病、大皰性表皮松解。
特別值得一提的是,今年3月,Mesoblast公司宣布,計劃在美國、澳大利亞、中國、歐洲評估Ryoncil治療由新型冠狀病毒(SARS-CoV-2)感染引起的急性呼吸窘迫綜合癥(ARDS)患者。該公司正在積極與政府和監管部門、醫療機構和制藥公司商討實施這些活動。
Ryoncil有潛力應用于急性呼吸窘迫綜合癥(ARDS)的治療,這是導致新型冠狀病毒肺炎(COVID-19)患者死亡的主要原因。這一點得到了在中國開展的一項由研究者發起的臨床研究的結果支持。該研究報告稱,使用同種異體MSC移植在所有7例COVID-19肺炎患者中治愈或改善了功能結果(詳細結果見2月28日上海大學、首都醫科大學等機構在中科院科技論文預發布平臺ChinaXiv上發表的文章:Transplantation of ACE2 -mesenchymal stem cells improves the outcome of patients with COVID-19 pneumonia)。
此外,在對60例慢性阻塞性肺疾病(COPD)患者隨機對照研究的事后分析中,Ryoncil輸注具有良好的耐受性,顯著降低炎癥生物標志物,顯著改善炎癥生物標志物升高患者的肺功能。由于新型冠狀病毒肺炎(COVID-19)中同樣的炎性生物標記物也升高,這些數據表明Ryoncil可能用于治療COVID-19引起的急性呼吸窘迫綜合癥(ARDS)。
人體感染新型冠狀病毒后,病毒快速復制和大量的促炎細胞因子、趨化因子反應破壞了肺微血管和肺泡上皮細胞屏障形成炎癥風暴,導致血管滲漏和肺泡水腫,肺部炎癥的加劇和彌漫性損傷,最終導致嚴重缺氧、進行性呼吸困難,乃至呼吸衰竭。
間充質干細胞(MSC)移植療法主要機理是,移植的異體間充質干細胞可合成和分泌抵抗多種微生物包括病毒的細胞因子,對微生物、各種炎癥、免疫反應進行可控的調節。同時,可合成和分泌多種血管和組織細胞生長因子促進受損血管和肺泡組織的恢復和重建,能迅速、顯著改善患者的預后,有效規避細胞因子風暴,為新冠肺炎患者的臨床治療提出了新思路。
“全世界并不是只有美國一個市場,只要拿得出讓人信服的數據,總會被認可的。”北京時間2月11日凌晨3點半,還有數萬名來自生物醫藥領域的從業者、投資者熬夜守候在直播間。他們正在線上圍觀一場醫藥評審會議。這......
2019年7月,美國食品藥品監督管理局(FDA)發布了關于抗病毒藥物產品提交二代測序數據的指南。指南為抗病毒藥物產品向FDA提交二代核苷酸序列分析程序以及支持耐藥性評估數據提供了意見。一、背景信息為保......
2020年4月1日,美國食品藥品監督管理局(FDA)發布了一份關于新型冠狀病毒肺炎(COVID-19)公共衛生緊急事件期間關于連鎖餐館和類似零售食品機構標準菜單中營養標簽的臨時政策。美國FDA法規要求......
MesoblastLtd是一家總部位于澳大利亞墨爾本的生物技術公司,是同種異體(通用型)細胞療法的全球領導者,致力于開發以細胞為基礎的再生治療產品,用于炎癥性疾病的治療。近日,該公司宣布,美國食品和藥......
孤兒藥(OphanDrug)是指用于診斷、治療和預防罕見病的藥品,而罕見病是一類發病率極低的疾病的總稱,又被稱為“孤兒病”。根據世界衛生組織(WHO)的定義,患病人數占總人口0.65‰~1‰的疾病即可......
......
2020年3月4日,美國食品藥品監督管理局(FDA)發布消息,該局發起了一項名為“FeedYourMind”的新教育計劃,以幫助消費者更好地了解轉基因食品。“FeedYourMind”計劃由美國農業部......
羅氏(Roche)近日宣布,美國食品和藥物管理局(FDA)已授予Esbriet(pirfenidone,吡非尼酮)治療無法分類的間質性肺病(uILD)成人患者的突破性藥物資格(BTD)。ILD是一種致......
2019年11月14日,美國食品藥品監督管理局(FDA)發布2019年自愿性國家零售食品監管項目標準(零售項目標準)(VoluntaryNationalRetailFoodRegulatoryProg......
日前,F2G公司宣布,美國FDA授予其首款候選藥物olorofim突破性療法認定,用于治療侵襲性真菌感染患者,包括難治型曲霉病患者,以及受多育孢子蟲(lomentosporaprolificans),......