我國醫藥工業是以仿制藥為主導的行業,但總體屬于低仿制水平,劣質或過剩產能亟需淘汰。目前我國通過GMP的藥企有5000多家,絕大多數是仿制藥企業,“小、散、亂”的現象比較突出。截止2016年底國家藥品食品監督局共批準18.9萬個藥品批文,但實際生產銷售的批準文號只有4萬-5萬個,意味著三分之二以上的文號是沒有實際生產的“僵尸文號”。大量國產仿制藥屬低水平仿制,與原研制劑相比安全低效甚至無效。因此,國家推出一致性評價政策的初衷也是為了淘汰過剩產能,淘汰僵尸批文,提高行業集中度以及行業利潤率,最終促進醫藥行業發展。
與此同時,2015年7月22日CFDA發布《關于開展藥物臨床試驗數據自查核查工作的公告》,掀起了臨床數據核查風暴。其中,涉及臨床的1622個品種由于臨床數據完整性問題不予批準占3%,在此重壓之下,企業主動撤回占77%,合計80%以上,且多家臨床基地與CRO被發現數據不完整性問題。因此,此前國內臨床數據存在不真實,不規范,不完整的情況,此次國家推出一致性評價政策正是要解決歷史遺留問題,一致性評價的執行代表著中國仿制藥行業新的起點,步入良性發展的道路。
更進一步,推行一致性評價利于推進供給側結構性改革。產品質量是供給側問題,是如何更好地滿足市場需求的問題,也是結構性問題。仿制藥質量提高了,臨床上實現與原研藥相互替代,就能夠推動藥品生產領域的結構性改革,改變現在原研藥在有的大醫院藥品銷售比達到80%的局面,有利于降低醫藥總費用支出,有利于淘汰落后產能,提高仿制藥的競爭力。醫藥企業通過開展仿制藥一致性評價,也有利于創新。制劑是有效成分、輔料和包材的有機結合,一致性評價將促進企業更多地進行生產工藝和輔料、包材的綜合研究,全面提高制劑水平。
1、一致性評價是提升我國仿制藥水平的基礎,品種通過后將享受國家政策鼓勵
仿制藥一致性評政策實施的目的在于仿制藥與ZL藥相比治療等效(Therapeuticequivalence,TE),可互相替代,一致性評價是仿制藥上市的基礎,從而免去大規模臨床試驗和研究。藥物制劑要產生最佳療效,其藥物活性成分應當在預期時間段內釋放吸收并被轉運到作用部位達到預期的有效濃度。大多數藥物是進入血液循環后產生全身治療效果的,作用部位的藥物濃度和血液中藥物濃度存在一定的比例關系,因此可以通過測定血液循環中的藥物濃度來獲得反映藥物體內吸收程度和速度的主要藥代動力學參數,間接預測藥物制劑的臨床治療效果,以評價制劑的質量。因此,仿制藥一致性價的通過需要完成藥學等效性與生物等效性兩個重要環節:
藥學等效性(Pharmaceuticalequivalence,PE):如果兩制劑含等量的相同活性成分,具有相同的劑型,符合同樣的或可比較的質量標準,則可以認為它們是藥學等效的。藥學等效不一定意味著生物等效,因為輔料的不同或生產工藝差異等可能會導致藥物溶出或吸收行為的改變。
生物等效性(Bioequivalence,BE):鑒于藥物濃度和治療效果相關,假設在同一受試者,相同的血藥濃度-時間曲線意味著在作用部位能達到相同的藥物濃度,并產生相同的療效,那么就可以藥代動力學參數作為替代的終點指標來建立等效性。以健康志愿者作為受試者,在相似的試驗條件下單次或多次服用相同劑量的試驗藥物后,通常采用藥代動力學終點指標藥物峰濃度Cmax和曲線下面積AUC來分別判定藥物的吸收速度和吸收程度與參比制劑的差異在可接受范圍內(幾何均值比值的90%臵信區間在80-125%之間)。
圖:一致性評價分為藥學等效性與生物等效性
圖:生物等效性評價的藥代動力學示意圖 資料來源:觀研天下整理

確定參比制劑與開展BE試驗是一致性評價的關鍵所在:
①參比制劑確定:既然仿制藥一致性評目的在于仿制藥與ZL藥相比治療等效,可相互替代,在開始一致性評價的首要環節就是確定參照的ZL藥即參比制劑。CFDA發布的供企業選擇參比制劑時參考清單分為已在中國境內上市和未在中國境內上市兩類,建議企業按以下順序選擇其一作為參比制劑備案:(一)原研藥品:進口原研藥品、經審核確定的原研企業在中國境內生產上市的藥品、未進口原研藥品;(二)在原研企業停止生產的情況下,可選擇美國、日本或歐盟獲準上市并獲得參比制劑地位的藥品。參比制劑的確定一般首先由仿制藥企業自行選擇并報國家一致性評價辦公室備案,60個工作日內無異議,即可以此備案試劑為參比試劑開始試驗。一致性辦公室會組織專家就備案、推薦和主動申報的參比制劑審核確定并及時公布。原則上,企業應當以CFDA公布的參比制劑為準,對CFDA已公布的參比制劑,建議企業按照公布的參比制劑開展研究,未備案的無需再備案。截止目前,CFDA共發布10批參比制劑目錄。
②BE試驗:根據國發20168號文規定,原則上通過生物等效性試驗(BE)進行一致性評價,符合BE豁免的品種,可采用體外溶出度方法進行一致性評價。BE等效性試驗是在相似的試驗條件下單次或多次服用相同劑量的試驗藥物后,受試制劑中藥物的吸收速度和吸收程度與參比制劑的差異在可接受范圍內,在正式開始BE試驗前,可根據預BE試驗情況,可能需要重新調整處方和工藝等藥學研究,能否通過生物等效性試驗將是通過一致性評價的最關鍵的環節。
圖:一致性評價的工作流程圖
資料來源:觀研天下整理
參考中國報告網發布《2018-2023年中國醫藥產業市場競爭態勢調查與未來發展方向研究報告》
仿制藥一致性評價的完成在一般情況下大概需要22-28個月,其中研究階段預計需要16-20個月,申報審批階段預計需要6-8個月。樂觀情況下,處方工藝不需要變更,或者方工藝不需要變更、BE獲得豁免的進行一致性評價品種進度較快。對于不能豁免BE的改處方工藝品種,提高BE試驗的成功率是關鍵。
另外,臨床資源缺乏也是影響一致性評價進程的關鍵因素。此前臨床試驗機構實行認定制,臨床試驗機構數量相對較少不能滿足大量仿制藥一致性評價需求,且并不是所有的臨床試驗機構可以承做BE試驗,因此臨床試驗機構成為各家仿制藥企業爭奪的稀缺資源。2017年8月25日CFDA發布了《總局關于仿制藥質量和療效一致性評價工作有關事項的公告》(2017年第100號),文中明確提出“對生物等效性試驗機構實行備案制管理。一致性評價中的生物等效性試驗可以在現有經認定的臨床試驗機構進行,也可以在其他具備條件的機構進行”,目前認定的臨床試驗機構共計619家。這一政策如能及時落地,或有望擴充臨床試驗資源,緩解一致性評價工作中臨床試驗資源匱乏的瓶頸。
表:一致性評價進程時間表
資料來源:觀研天下整理
據8月25日CFDA發布的《關于仿制藥質量和療效一致性評價工作有關事項的公告》,一致性評價申請獲得受理后評審時限為120個工作日(立卷45+核查60+綜合意見15),需申請人補充資料的,申請人應在4個月內一次性完成補充資料。總局通過文件形式明確了較短的評審時間,鼓勵了相關仿制藥企業對于一致性評價的積極性。
圖:一致性評價評審流程

資料來源:觀研天下整理
仿制藥通過一致性評價后將被納入《中國上市藥品目錄集》并可在藥品標簽、說明書中使用通過一致性評價標志,同時國家將在醫保支付、集中采購,技術與資金等方面對通過品種給予政策支持:
1)醫保支付方面:通過一致性評價的藥品品種,社會保障部門將在醫保支付方面予以適當支持,有關部門將加快按通用名制訂醫保藥品支付標準,盡快形成有利于通過一致性評價仿制藥使用的激勵機制,醫療機構應優先采購并在臨床中優先選用。
2)集中采購方面:同品種藥品通過一致性評價的生產企業達到3家以上的,衛生計生部門在藥品集中采購等方面不再選用未通過一致性評價的品種;未超過3家的,優先采購和使用已通過一致性評價的品種。
3)技術與資金支持方面:通過一致性評價藥品生產企業的技術改造,在符合有關條件的情況下,可以向發展改革、工信和財政等部門申請中央基建投資、產業基金等資金支持。此外,國家食品藥品監督管理總局鼓勵具有上市許可持有人資格的企業,將通過一致性評價的藥品委托其他生產企業生產,以擴大產量,滿足市場需要。我們預計上述醫保支付、優先采購等配套政策有望于明年一季度在第一批品種通過一致性評價后出臺,因此在可預期的時間范圍內有望享受相關政策紅利,對相關企業帶來業績的增厚。
圖:通過一致性評價的標志
資料來源:觀研天下整理
2、確定首批進行一致性評價的基藥目錄中289個口服固體制劑品種,2018年底前完成
2016年3月5日國務院辦公廳印發《關于開展仿制藥質量和療效一致性評價的意見》(國辦發20168號),文中提出需要進行一致性評價的品種范圍以及首批限定時間需要完成一致性評價的品種目錄:
1)化學藥品新注冊分類實施前批準上市的仿制藥,無論是國產仿制藥,還是進口仿制藥、原研藥品地產化品種,凡未按照與原研藥品質量和療效一致性原則審批的,均須開展一致性評價。
2)首批將對國家基本藥物目錄(2012年版)中2007年10月1日前批準上市的化學藥品仿制藥口服固體制劑(共計289個品種)進行一致性評價,這部分藥品原則上應在2018年底前完成一致性評價。
3)上述以外的其他化學藥品仿制藥口服固體制劑,企業可自行組織一致性評價工作,自首家品種通過一致性評價后,三年后不再受理其他藥品生產企業相同品種的一致性評價申請。除了以上這些仿制藥以外的其他化學仿制藥,包括基本藥物目錄中其它劑型的藥品,非基藥目錄的品種等等,由于涉及品種眾多、情況復雜,國家食品藥品監管總局將分期分批發布開展質量和療效一致性評價的品種名單。
為什么首先要對基本藥物目錄中的化學藥品口服固體制劑進行一致性評?我們認為主要有以下兩點原因:一是因為口服固體制劑量大面廣、最為常用;二是基本藥物是保障群眾基本用藥需求的品種。根據CFDA初步統計,2007年10月前批準上市的化學藥品仿制藥口服固體制,在基藥目錄中有289個品種、17740個批準文號或注冊證號,涉及1817家國內生產企業、42家進口藥品企業。
根據米內網數據統計,2016年289個一致性評價品種在醫院端銷售規模約614億元,占醫院化學藥市場規模約6%。其中,消化系統及代謝用藥、心血管系統藥物、血液和造血系統藥物、全身抗感染藥物的銷售規模排名靠前,分別為148億元、128億元、108億元、95億元。血液和造血系統藥物、心血管系統藥物單品種、消化系統及代謝用藥的單品種銷售額較大,分別為12億元、3.76億元、2.79億元。
圖:289個一致性評價品種市場規模VS化學藥醫院市場規模
資料來源:觀研天下整理
表:289個一致性評價品種疾病治療領域格局
資料來源:觀研天下整理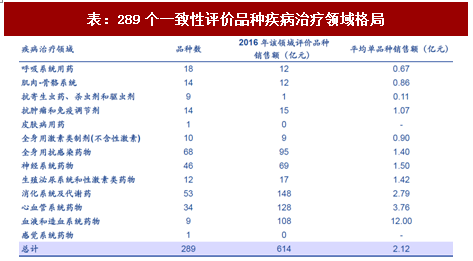
從各層級醫療機構289個一致性評價品種市場規模角度來看,城市公立醫院金額占比最大,2016年實現銷售額340.6億元,占比55.5%,其次是縣級公立醫院,實現銷售116.6億元,占比20%。從289個一致性評價品種的內外資格局角度來看,外資品牌在城市公立醫院以及城市社區衛生服務中心(站)占主導地位,而國產品牌在縣級公立醫院以及鄉鎮衛生院占主導地位。
表:各層級醫療機構289個一致性評價品種市場規模(億元)及內外資格局
資料來源:觀研天下整理
經國家藥品監督管理局仿制藥質量和療效一致性評價專家委員會審核確定,現發布仿制藥參比制劑目錄(第九十三批)。特此通告。附件:化學仿制藥參比制劑目錄(第九十三批)國家藥監局2025年7月7日......
2025年02月27日,河北藥監局發布了關于印發《2025年全省藥品監督管理工作要點》的通知,通知中對專業化監管隊伍、促進京津冀協同發展、深化藥品監管改革、建立約談管理辦法、推進仿制藥一致性評價、優化......
2025年02月27日,河北藥監局發布了關于印發《2025年全省藥品監督管理工作要點》的通知,通知中對專業化監管隊伍、促進京津冀協同發展、深化藥品監管改革、建立約談管理辦法、推進仿制藥一致性評價、優化......
國家藥監局關于發布仿制藥參比制劑目錄(第九十批)的通告(2025年第9號)經國家藥品監督管理局仿制藥質量和療效一致性評價專家委員會審核確定,現發布仿制藥參比制劑目錄(第九十批)。特此通告。國家藥監局2......
2025年2月9日,國家醫保局聯合藥監部門針對集采藥品質量問題的爭議給出明確回應,并提出一系列優化監管措施,希望消除公眾疑慮,確保藥品集中帶量采購政策(簡稱“集采”)的平穩推進,讓患者用上“低價優質藥......
近日,第十批國家組織藥品集中帶量采購的擬中選結果公布,部分國產仿制藥以極低價格中選,引發了廣泛關注。其中,阿司匹林腸溶片的最低中標價僅為3分錢一片。與此同時,流感高發期的到來使得抗流感藥物需求激增。盡......
近日,第十批國家組織藥品集中帶量采購的擬中選結果公布,部分國產仿制藥以極低價格中選,引發了廣泛關注。其中,阿司匹林腸溶片的最低中標價僅為3分錢一片。與此同時,流感高發期的到來使得抗流感藥物需求激增。盡......
國家藥監局關于發布仿制藥參比制劑目錄(第八十四批)及調出參比制劑目錄品種清單(第一批)的通告(2024年第46號)經國家藥品監督管理局仿制藥質量和療效一致性評價專家委員會審核確定,現發布仿制藥參比制劑......
藥品包裝上的通用名常顯著標示,單字面積大于商品名的2倍;在橫版標簽上,通用名在上1/3范圍內顯著位置標出(豎版為右1/3范圍內);字體顏色使用黑色或者白色。藥品包裝上的商品名一般與通用名分行書寫,其單......
國家藥監局關于發布仿制藥參比制劑目錄(第八十四批)及調出參比制劑目錄品種清單(第一批)的通告(2024年第46號)經國家藥品監督管理局仿制藥質量和療效一致性評價專家委員會審核確定,現發布仿制藥參比制劑......