近十年來,液體活檢研究熱度不斷攀升,多個國家以及地區的研究紛紛投入其中。
一、傳統腫瘤檢查之“痛”
如果某人不幸確診患上惡性腫瘤,似乎將面臨無盡的“痛苦”和“危險”。除了各種治療方法要“折磨”他的身體,各種定期檢查、藥物療效評估方法也給病人帶來了巨大的“痛苦”。
整個腫瘤診療過程,從篩選到初步診斷,到手術診療,再到放化療,病人都離不開影像檢查和病理活檢。其中,病理檢查是腫瘤診斷的“金標準”,醫生會根據腫瘤位置、發病階段等因素選擇穿刺或手術采集腫瘤標本,制成病理切片活檢,進行診斷或病情評估。不過,這種傳統的檢查方式存在局限性,例如:
部分病灶體積太小,影像學檢查難以準確定位,醫生無法操作活檢,不得不讓患者等待一段時間(有時候甚至是幾個月)再來檢查,導致病情延誤;
部分病灶無法穿刺(例如肝臟、大腦部位腫瘤)取樣;
手術采集腫瘤標本,給患者帶來很大痛苦,并且不能頻繁進行,因此不便用于持續性腫瘤監測;
傳統活檢手段往往只能監測單一器官,不適合常規體檢使用;
直接從腫瘤提取組織可能進一步刺激腫瘤,激發癌細胞快速增長。
血液檢查則提供了另一種備選方案。通過測定某些血液腫瘤標志物(通常是蛋白,例如癌胚抗原CEA、腫瘤特異性生長因子TSGF、甲胎蛋白AFP),可以快速診斷腫瘤存在狀態、生長情況,效率大大提升,診斷方式更加便捷。
然而血液腫瘤標志物同樣具有一些限制,包括:
假陽性率高。部分腫瘤標志物在特定正常生理情況或良性疾病下也可以異常升高。
穩定性差。腫瘤標志物容易受到生理狀態影響,波動性大。腎功能衰竭、風濕病、吸煙、酗酒、服用藥物等均可能導致濃度增高。
一種腫瘤標志物往往與多種腫瘤相關,同樣一種腫瘤也可能引起多種腫瘤標志物升高。
假陰性率高。腫瘤標志物正常,并不能排除腫瘤發生。有的腫瘤自始至終腫瘤標志物都不升高,有的腫瘤其早期標志物正常,疾病進展后才升高。
液體活檢技術的出現,彌補了上述的一些缺點。腫瘤的監測、用藥評估等方面,液體活檢技術大大提高了檢測時效性和準確性,在一定程度上減輕了腫瘤患者的“檢查之痛”。
二、液體活檢是什么
液體活檢技術,實質上是體外診斷中的分子診斷技術,在樣本來源上的延伸(從組織延伸至血液、體液、外泌體等,臨床更多采用血液),通過檢測腫瘤或轉移灶釋放到血液循環中的腫瘤細胞(CTC)和腫瘤DNA(ctDNA)碎片,早期篩查、檢測腫瘤,或評估藥物療效等。由于其非侵入式取樣特性,是檢測腫瘤、輔助治療的突破性技術,是“精準醫療”代表性的診斷技術。
表1 腫瘤標志物檢測和液體活檢的區別

三、 液體活檢的應用方向
液體活檢技術可應用于腫瘤的早期篩查、檢測、用藥指導、評估、觀察,貫穿癌癥診治全程,同樣是液體活檢技術的核心優勢之一。
1.腫瘤篩查:當腫瘤生長到一定階段,會向血液循環釋放腫瘤細胞(CTC)或者腫瘤DNA(ctDNA,CTC和ctDNA將在后續文章中詳細介紹),通過檢測它們有助于篩查腫瘤。
2.腫瘤分期分級:循環系統是腫瘤轉移的重要途徑,如果將外周血CTC計數和染色作為臨床分期的參考條件,可增進對腫瘤分期的理解,有利于醫生制定腫瘤治療方案。另一方面,在癌癥突變的不同階段,CTC含量和ctDNA突變情況都可能會不同,有助于醫生判斷病人的腫瘤進展。
3.預后評估:癌癥患者接受治療有效,CTC數量將會相應減少;療效欠佳,CTC數量變化很小。因此血液CTC含量變化可以幫助判斷治療效果,了解病人耐藥情況和疾病進展,進一步調整治療方案。
4.精準用藥(個體化治療):同一種癌癥,突變仍然可能不同,對不同藥物反應各異。FDA目前已經批準了大量根據腫瘤基因型突變的癌癥個性化用藥指導方針。傳統上利用腫瘤組織活檢或手術取得的組織標本檢測腫瘤基因突變。目前研究表明,ctDNA突變與腫瘤組織突變具有高度相似性,分析血液ctDNA可以幫助醫生判斷病人腫瘤的突變類型,制定用藥方案。
5.耐藥監控:腫瘤患者接受一段時間化療治療后,相當一部分會出現耐藥。過去只能在化療隨診時才能回顧性評價,且傳統組織活檢只能檢測腫瘤組織局部區域,不能反應腫瘤的動態變化。近年來,越來越多研究表明,檢測患者外周血ctDNA突變類型的變化,可能是實時監測腫瘤藥物耐藥一種非常有效的方法。
6.腫瘤轉移、復發:腫瘤轉移和復發是腫瘤致死的主要原因,多數腫瘤若能早期檢測到轉移、復發,患者還有較大的治療機會。但傳統影像學檢測對腫瘤轉移和復發的早期預警靈敏度和及時性尚有不足。癌癥復發早期,血液CTC、ctDNA即增加。
四、液體活檢的市場規模
1.全球市場規模預測
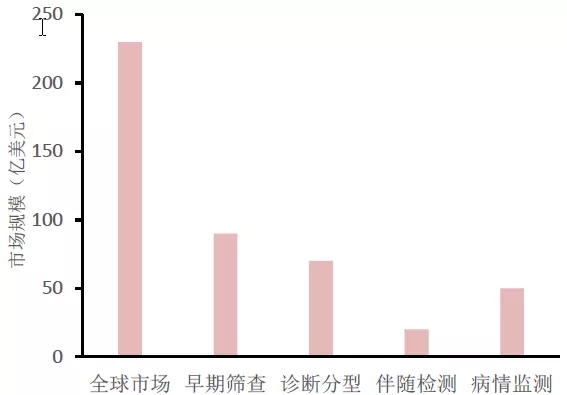
圖2 國際液體活檢全球市場規模(億美元)
資料來源:GoldmenSachs Report,浙商證券研究所
高盛將液體活檢分為早期篩查、診斷分型、伴隨檢測和病情監測四個領域,預計全球市場潛力可達230億美元,并預測市場需要5-15年才能快速發展并成熟。
2.中國市場規模預測
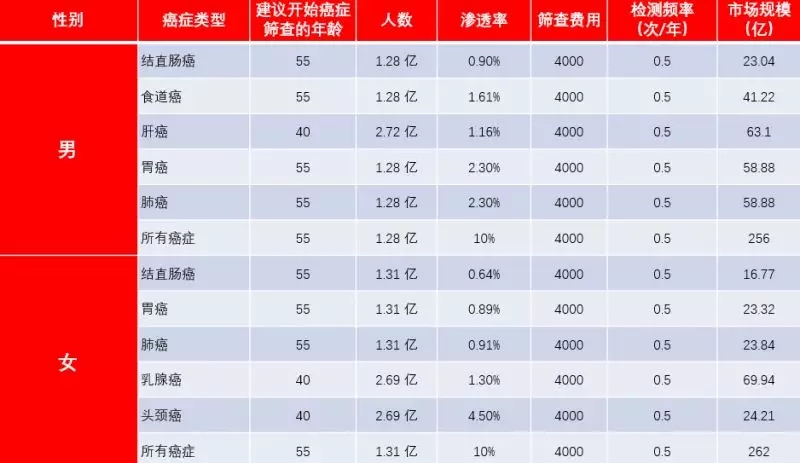
圖3 中國液體活檢癌癥早期篩查市場規模預測
資料來源:GoldmenSachs Report,浙商證券研究所
預計未來癌癥早期篩查市場規模約在518億元人民幣,其中男性肝癌、胃癌和肺癌未來市場空間較大,而女性乳腺癌由于發病年齡早,發病率高,是未來癌癥早期篩查市場空間最大的瘤種。
結合目前液體活檢發展的勢頭來看,雖然液體活檢在癌癥治療市場份額相對較小,但對腫瘤患者而言是“剛需”。預計未來2-5年內,這部分市場會率先開始發展。早期篩查市場雖然空間大,但是目前技術尚未達到臨床需求,而且價格高,客戶接受程度低,推廣困難。技術突破和成本降低是腫瘤早期篩查市場的催化劑。
最后,強調兩點內容:
1.液體活檢尚不能用于腫瘤早篩。早篩是指對腫瘤的預測,以及早期腫瘤的檢查。因為只有當腫瘤生長到一定階段后,CTC或者ctDNA進入血液,才能通過液體活檢的方式檢測出來。而此時,腫瘤往往已經生長到一定規模,不再是早期腫瘤了。
2.液體活檢技術不是傳統檢查的替代技術。腫瘤的初步診斷、確診和療效評估,應該根據實際情況,結合影像、腫瘤標志物和液體活檢等檢查方式綜合判斷。液體活檢在一定程度上解決了傳統技術的部分局限性,但尚不足以替代傳統檢測技術。
液體活檢專題(二)——技術分類
一、液體活檢的技術分類
目前,液體活檢主要包括CTC(circulatingtumor cells,即循環腫瘤細胞)檢測、ctDNA(circulatingtumor DNA,循環腫瘤DNA)檢測和外泌體(Exosome)檢測三類技術。
圖1 液體活檢分類
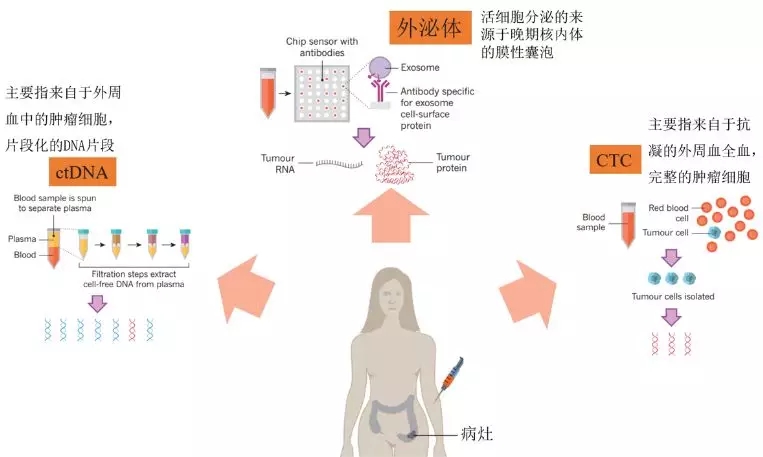
資料來源:浙商證券研究所
圖2 各類液體活檢技術的區別
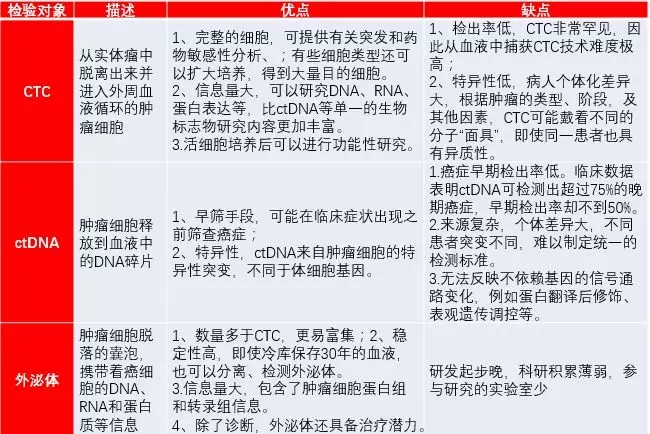
二、液體活檢各類技術的研究情況
1.CTC檢測的臨床研究統計
截至2018年4月13日,全球共有CTC檢測相關研究589項,其中美國259項,中國96項。地區分布如下:
圖3 全球CTC檢測研究分布
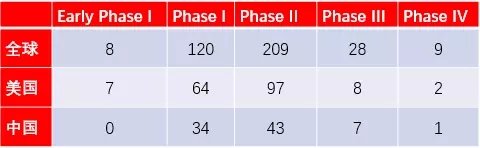
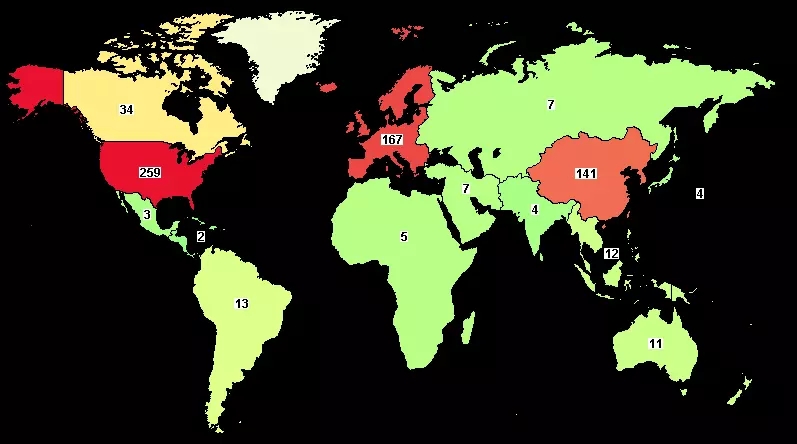
資料來源:ClinicalTrails
2.ctDNA檢測的臨床研究統計
截至2018年4月13日,全球共有ctDNA檢測相關研究212項,其中美國56項,中國30項。地區分布如下:
圖4 全球ctDNA檢測研究分布
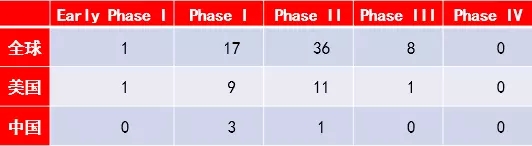
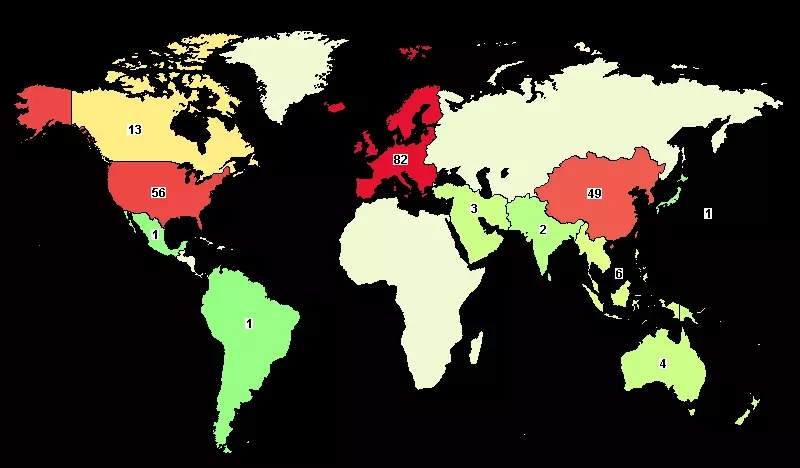
資料來源:ClinicalTrails
3.外泌體檢測的臨床研究統計
截至2018年4月13日,全球共有外泌體檢測相關研究77項,其中美國26項,中國6項。地區分布如下:
圖5 全球外泌體檢測研究分布
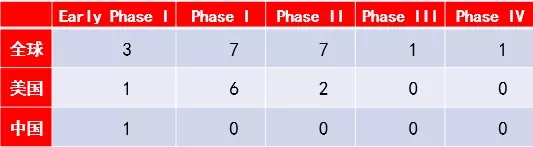
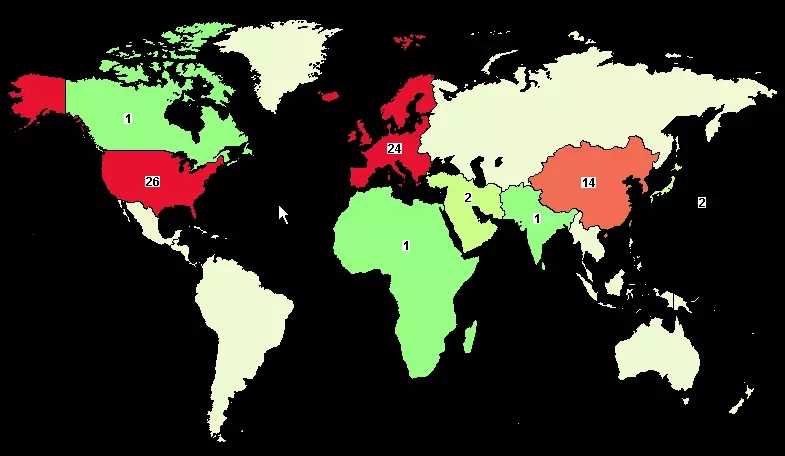
資料來源:ClinicalTrails
上述數據表明,研發進度上CTC>ctDNA>外泌體,北美>西歐>東亞,未來北美和歐洲依然將是液體活檢研究和應用最活躍的地區。
CTC檢測的臨床研究最多,技術最成熟,未來可能首先實現產業化。目前全球已有9個CTC的四期(上市后)臨床實驗,預計1-2年內會有更多CTC檢測產品面世。ctDNA研究相對較少,臨床研究主要處于一期和二期,預計2-3年后產品才會逐漸上市。外泌體研究起步晚,臨床研究非常少,僅有1例四期臨床的實驗。
目前國內進行CTC、ctDNA檢測的液體活檢公司數十家,基于組織活檢的基因檢測公司則數量眾多。但是,具有臨床試點資質的醫院較少,樣本資源有限,成為各大公司爭搶的對象。未來液體活檢將面臨一個大的整合階段,那些能夠占領渠道和臨床資源的公司勢必在競爭中處于優勢地位,并有望通過整合其他公司而發展壯大。
三、國內外液體活檢產品的審批情況
1.美國液體活檢產品審批情況
FDA目前僅批準了三款液體活檢相關產品,分別是楊森診斷公司(Janssen Diagnostics)的Cell Search(基于CTC檢測),Epigenomics公司的Epipro Colon技術(基于ctDND檢測),以及羅氏的cobas EGFR突變檢測試劑盒v2。
圖6 美國批準的第一個CTC 檢測系統--CellSearch

資料來源:CellSearch 說明書,浙商證券研究所
圖7 美國批準的第一個ctDNA 檢測產品--EpiproColon
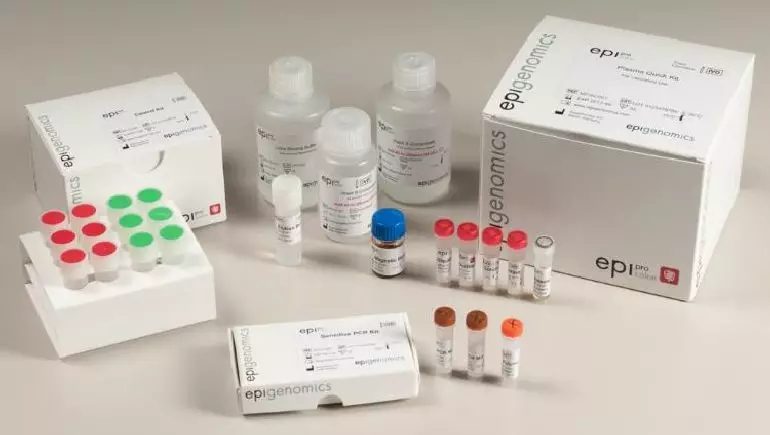
資料來源:EpiproColon 說明書,浙商證券研究所
圖8 cobas EGFR 突變檢測試劑盒v2
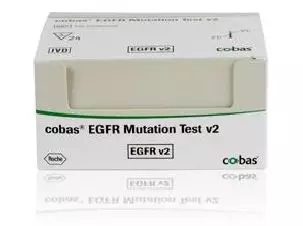
資料來源:浙商證券研究所
(1)CellSearch
美國FDA在2004年、2007年和2008年分別批準CellSearch 系統用于轉移性乳腺癌、結直腸癌與前列腺癌的預后評估、無進展生存期和總生存期預測。我國CFDA在2012年批準了CellSearch 系統用于轉移性乳腺癌的預后評估。雖然目前市場上的CTC檢測儀器很多,但是這是唯一一款通過FDA認證的儀器。
(2)EpiproColon試劑盒
2016年4月,美國FDA批準了Epigenomics公司以血液為基礎篩查結直腸癌的EpiproColon技術。結直腸癌病人Septin9基因V2區域的胞嘧啶會發生甲基化,而正常人不發生。外周血Septin9基因發生的甲基化可以通過DNA的特異擴增檢測。EpiproColon(Septin9基因甲基化檢測試劑盒)能檢測血液中Septin9基因V2區域發生甲基化的CpG島bisDNA序列。臨床數據顯示EpiproColon可檢出68%的病例。這是FDA批準的第一款基于ctDNA進行腫瘤篩查的產品。
(3)cobasEGFR突變檢測試劑盒v2
這是一款以血液為基礎、伴隨抗癌藥特羅凱(Tarceva,通用名:erlotinib,厄洛替尼)治療的診斷試劑盒。采用cobasEGFR Mutation Test v2檢測患者血液樣本中存在的特定NSCLC突變(外顯子19刪除或外顯子21[L858R]置換突變,10-20%的NSCLC病例存在這類突變)幫助鑒別可能從特羅凱(Tarceva)治療受益的患者。這是FDA批準的首個以血液為基礎、用于檢測非小細胞肺癌(NSCLC)患者表皮生長因子受體(EGFR)基因突變的檢測試劑盒。
2. 中國液體活檢產品審批情況
中國市場方面,CFDA目前除批準了楊森診斷公司(JanssenDiagnostics)的Cell Search以外,僅批準了三個國內產品:(1)格諾思博公司的葉酸受體陽性CTC檢測試劑盒;(2)友芝友公司的循環腫瘤細胞快速染色液;(3)艾德生物的ctDNA檢測試劑盒
圖9 CFDA 批準的第一個CTC檢測試劑盒—CytoploRare

資料來源:格諾思博,浙商證券研究所
圖10 CFDA 批準友芝友公司的循環腫瘤細胞快速染色液

資料來源:友芝友公司官網,浙商證券研究所
圖11 艾德生物的人類EGFR突變基因檢測試劑盒(Super-ARMS?)
資料來源:艾德生物官網
從中國和美國液體活檢的產品來看,液體活檢總體來說還處在萌芽期,產品很少,市場尚未打開。主要的新產品都在近年才公布,可以說未來還有很大的發展空間。
液體活檢專題(三)——產業鏈和行業問題
近幾年,液體活檢概念比較火爆,屬于熱門投資領域。有沒有朋友好好想想,這個領域可能存在一些問題?
一、液體活檢行業的產業鏈
液體活檢行業的產業鏈可以描述為:上游器械、原材料——中游產品生產——下游數據處理。
1.上游器械和原材料產品技術壁壘高
器械主要包括CTC分析儀、數字PCR儀、二代測序儀等,試劑盒的關鍵原材料是抗體和芯片。這些儀器和原材料的生產技術壁壘很高,ZL保護嚴格,國外公司(賽默飛世爾、奧林巴斯等)形成了高度市場壟斷。國內已有幾家公司通過并購實現二代測序儀的生產,但產品性能與國外產品相比差距較大,產品同質化嚴重,競爭激烈。
2.中游企業
中游試劑盒生產企業數量較多,競爭激烈。上期文章已經分析了國內外目前在研產品數量。國內友芝友、益善生物等企業的液體活檢產品已經獲得CFDA上市審批,產品均為I類或者II類器械。
3.下游企業
下游主要考慮兩個要素:一是銷售能力,由于液體活檢并不是主要的腫瘤檢驗方式且價格偏高,受眾規模小,醫院采購量有限,有渠道進入醫院的企業可以“占山為王”,因此中游企業對銷售渠道的依賴比較嚴重;二是數據解讀分析能力,解讀準確度高、速度快的產品必定更受市場青睞。
該類產品尚不能進入醫保目錄是制約銷售的關鍵因素。醫院要考慮“藥占比”,液體活檢產品高昂的價格,導致其進入公立醫院必然面臨重重困難。因此很多產品都是進入了非公立的腫瘤治療中心、民營醫院、第三方檢驗中心等機構,銷售數量有限。
二、液體活檢行業面臨的主要問題
1.液體活檢僅被看作是組織活檢的替補方案
患者如何在液體活檢和組織活檢之間選擇,取決于檢查的目的是什么。初始診斷優先選擇組織活檢,只要患者能夠提供足夠的組織樣本;如果組織樣本不足量,液體活檢可以是替補方案。因此,液體活檢不會替代其他檢查方式,也難以搶占傳統活檢的市場份額。
2.假陰性問題
如果液體活檢的結果為陽性,可以作為制定治療方案的依據之一。問題在于,陰性結果能否采納需要進一步驗證。許多腫瘤的CTC、ctDNA數量不足或者腫瘤存在明顯異質性,導致腫瘤即使突變,液體活檢試劑盒也不一定能捕捉到CTC或ctDNA,血液檢查結果也可能為陰性。因此,液體活檢難以用于早篩,更多用于腫瘤中后期(IV期以后)的治療效果評價(但是這個結論,目前也被第4條中的一篇綜述文獻推翻了)。
3.價格高,暫時不能進醫保目錄,推廣難度大
低通量液體活檢產品價格低廉,但是檢出率也較低,應用前景有限。高通量產品對部分腫瘤的檢出率高達80%-90%,但價格偏高。以華大基因個性化診療檢測Oseq-T/ctDNA為例,該產品可一次性檢測508個基因,并解讀100種抗腫瘤藥物和基因變異的關系(包含化療藥物26種,已經獲FDA批準靶向藥物47種以及正在進行臨床III/IV期試驗藥物27種),靈敏度、特異性高達99%,產品官網標價14800元/次。患者整個治療過程平均要檢查3-4次,液體活檢費用在5-8萬元左右。國內部分廠家的CTC檢測產品,單次檢查費用在5000-8000元左右,整個療程檢查總費用近5萬元。同時,這類產品尚未納入醫保目錄,普通民眾較難獨立接受如此高昂的價格。
4.對cfDNA產品的可靠性質疑
年初,美國臨床腫瘤學會(ASCO)在《Journalof Clinical Oncology》雜志發表了一篇題為“Circulating Tumor DNA Analysis in Patients With Cancer: American Society of Clinical Oncology and College of American Pathologists JointReview”的綜述文章,對ctDNA的分析有效性、臨床有效性和臨床實用性提出質疑。調查結果顯示:(1)以前的部分研究指出,ctDNA更適合用于晚期癌癥的篩查,而非用于臨床早篩,但是目前看來,即使用于晚期癌癥,其有效性和合理性也沒有足夠的證據來證明;(2)還沒有足夠的證據支持常規使用ctDNA檢測早期癌癥,并以此做出治療決策、監測治療效果、尋找殘留癌細胞;(3)液體活檢與組織檢測經常結果不一致,因此陰性液體活檢結果應與腫瘤組織基因分型對比確認。文章強調,ctDNA檢測結果必須與其他信息結合,才能為患者提供最佳選擇。
因此,液體活檢技術,對于資本圈而言是makesense,對于醫學界而言,可能是nosense!那么,這個領域真正的商業化價值會是什么?(個人認為可能是單個瘤細胞的捕獲和分離,用于后期繼續研究。僅代表個人觀點,持不同意見的朋友歡迎討論)
液體活檢的三個領域中(CTC、ctDNA和外泌體的檢測),CTC檢測產品技術更為成熟,部分產品已經上市銷售。ctDNA產品的性能近期頻受質疑,外泌體則處于早期研發階段,尚未有企業推出產品。
GeneCentricTherapeutics周三宣布完成800萬美元C輪首輪融資,以支持其GenomicsNext循環腫瘤DNA(ctDNA)液體活檢平臺的推出和商業化。此次融資由HatterasV......
近日,中國科學院大連化學物理研究所研究員樸海龍與中山大學腫瘤防治中心鞠懷強教授、徐瑞華教授團隊合作,建立了基于血清脂質組學的胃癌診斷與預后分型高性能機器學習模型,能夠根據病人的血清脂質組學數據對病人是......
血漿中無細胞DNA(cfDNA)是機體所有器官細胞死亡的非侵入性生物標志物,解析cfDNA的組織來源或能幫助揭示因疾病所致的異常細胞死亡,這在疾病檢測和監測上或許有著巨大的臨床潛力;盡管前景廣闊,但由......
科技日報記者劉霞實習生喬宇彤美國科學家近日在《公共科學圖書館·綜合》雜志發表研究報告稱,他們使用伴侶蛋白作為血液中癌細胞的新標記物,更清晰地觀察到了癌癥的擴散情況。通過使用這種新標記物,科學家們能夠在......
活檢又稱為無創診斷技術,是通過采集人體血液、積液、尿液、唾液等體液樣本,檢測體液液體樣本生物標志物進行腫瘤分析的診斷技術。作為現代精準醫療的核心技術之一,液體活檢具有覆蓋范圍廣、成本低、安全性高等優勢......
液體活檢是近幾年來興起的一種分子檢測手段,可以幫助臨床醫生早期篩查和發現腫瘤,為腫瘤的早期診斷提供了一種比常規腫瘤標志物靈敏性及特異性更高的替代方法。同時,液體活檢還具有實時監測治療療效和耐藥基因的產......
癌癥對每個人和家庭來說都是一場災難,對國家來說是一筆極大的公共衛生項目支出,根據2019年國家癌癥中心發布的中國惡性腫瘤流行情況分析報告顯示,隨著惡性腫瘤發病數持續上升,我國每年所需的相關醫療花費超過......
伴隨著中國老齡化的加速,“帶瘤生存”和新發癌癥比例正逐漸上升。癌癥早篩早檢在國內進入了黃金時期。10月11日,基準醫療(AnchorDx)與美國著名基因公司TwistBioscience(拓維思特,納......
癌癥已成為對人類生命健康的危險之一,死亡率和發病率持續升高。液體活檢作為新興的腫瘤診斷技術,因其無創性、敏感性、操作便捷等優勢受到關注。液體活檢使用的生物標記物主要有循環腫瘤細胞(CTCs)、細胞外囊......
科學家分析了血液中循環的腫瘤DNA的短片段。這種液體活檢分析利用了骨腫瘤獨特的表觀遺傳學原理,并且不依賴于任何遺傳改變,而這種改變在兒童期癌癥中很少見。這種方法有望改善個性化診斷,并可能改善諸如尤因肉......