抗體藥發現的兩大礦場
抗體藥主要有兩個大礦場,一個是依賴于體外展示技術的全合成/半合成/天然抗體文庫礦,比較耳熟能詳的是劍橋抗體技術公司(藥王阿達木單抗)、后來的Dyax和現在的MorphoSys(特諾雅?古塞奇尤單抗注射液)。著名的礦主有2018年諾貝爾化學獎得主溫特爵士(噬菌體展示平臺)和MIT教授、AdiMab聯合創始人K. Dane Wittrup教授(酵母展示平臺)。另一個礦是基于天然免疫系統的抗體發現。最初大家都是用野生鼠免疫結合雜交瘤技術來發現抗體,后來基因泰克的卡比利ZL以及各種鼠源抗體人源化技術壁壘逼迫一些科學先驅另辟捷徑,這就開啟了人源化抗體鼠的時代。比較知名的有Xenomouse(安進的技術平臺),Velocimouse(再生元的技術平臺)、國內最近出現的百奧賽圖的RenMabTM鼠以及和鉑醫藥的H2L2鼠。
從基因泰克的發展看抗體藥成藥性如何突破?
經過二十多年的發展,基于體外展示技術和合成抗體文庫的體外抗體發現撞了成藥性這個墻。最近七、八年整個領域都在反思到底問題出在哪里,到底該怎么尋求突破?在對全合成抗體的成藥性的質疑聲越來越強的時候,業內大佬們也在抓緊時間布局。
您是否注意到最近四五年基因泰克在抗體發現上全面轉向了基于單細胞技術的體內抗體發現。這是為什么呢?基因泰克在上世紀九十年代的抗體工程非常卓有成效,上市了美羅華(Rituxan)、曲妥珠(Herceptin)等抗體藥。但從2000年開始大量投入基于噬菌體展示技術的高通量篩選以后,新藥產出效率卻大大下降。基因泰克將何去何從?通過對一篇文章的解讀大家一起來看一下。
這篇文章(Hotzel I et al, 2013 mAbs)由基因泰克Paul Carter和Robert Kelley一起發表,文章中要解決的問題只有一個:噬菌體展示出來的抗體在藥物動力學(Pharmacokinetics)上是不是比人源化抗體差?
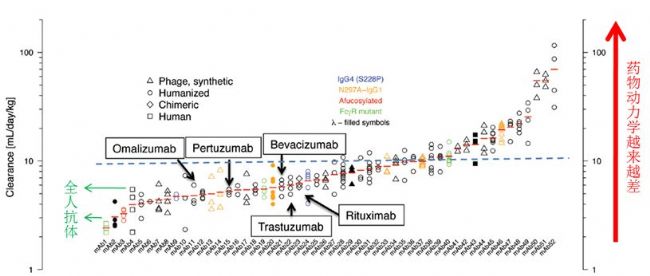
Fig. 1 52個抗體藥物及在研抗體在食蟹猴中清除速率的回溯性研究
圖Fig.1中Y軸是單抗藥在食蟹猴體內的清除速率(mL/day/kg),數值越大則藥物動力學越差。X軸是52個已經上市或者是在研的抗體藥物,包括大家耳熟能詳的貝伐珠單抗、美羅華單抗、曲妥珠單抗、奧馬珠單抗和帕妥珠單抗。在食蟹猴體內的清除速率10mL/day/kg(圖中藍色虛線)可以做為一個藥物動力學好壞的分界值。
噬菌體展示來的抗體(△)在食蟹猴體內的清除速率的中位值是9.0mL/day/kg,人源化抗體(?)在食蟹猴體內的清除速率的中位值是6.5mL/day/kg,作者表示在統計學上并無顯著性差異(P=0.28)。作者并沒有做兩者跟全人抗體的比較,可能由于全人抗體數據較少,但從有限的全人抗體數據來看,全人抗體(□)在食蟹猴體內的清除速率的中位值大概是3.1mL/day/kg,大家可以自行做個比較判斷(Fig
2a)。雖然文中沒有特意做數據差異比較,但相信這個發現應該也讓Paul Carter和Robert
Kelley非常震驚。因為基因泰克在2013年以后在抗體發現技術路線上的布局發生了變化,他們開始摒棄基于噬菌體展示的全合成抗體發現,并且大力投入基于單細胞抗體發現技術的體內抗體發現。
當然藥物動力學是個很復雜的東西,影響因素很多,雖然此研究可能某方面不夠嚴謹,但對于做商業決策來說,已經足夠高大上了,基因泰克抗體發現理念也是非常讓人贊同:那就是在抗體發現的早期來解決成藥性問題。
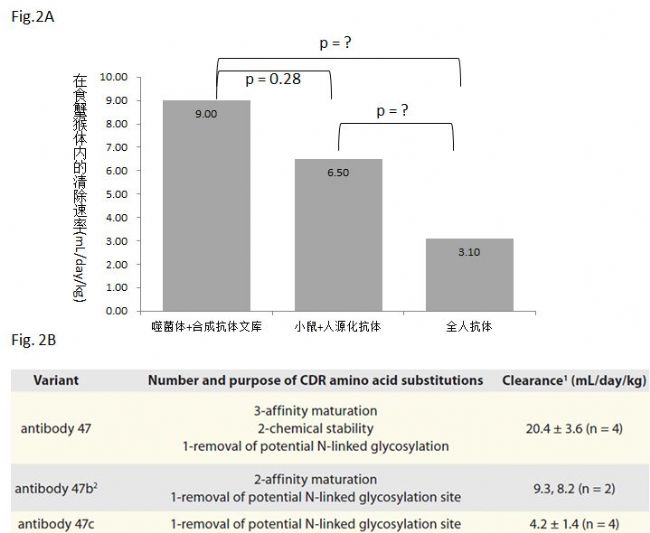
Fig. 2. 抗體人源化以及親和力工程改造對藥物動力學的影響
這篇文章還有一個非常有意思的數據,Paul Carter和Robert
Kelley選用了一個抗體(抗體47)來說明抗體工程化改造對體內藥物動力學的影響。抗體47是基因泰克早期發現的一個抗人成纖維生長因子的抗體,經小鼠免疫獲得。圖Fig.
2B,抗體47c相對于原生抗體序列來說只除去了一個潛在的糖基化位點,在食蟹猴體內的清除速率是4.2 mL/day/kg
(n=4)。抗體47b是在47c的基礎上又做了親和力優化,在食蟹猴體內的清除速率分別是9.3和8.2 mL/day/kg
(n=2)。抗體47是在47c的基礎上做了親和力優化和化學穩定性優化,在食蟹猴體內的清除速率是20.4 mL/day/kg
(n=4)。這個數據充分說明了一個問題,那就是經過體內免疫系統所發現的抗體的藥物動力學是最好的,體外的工程學優化對于體內的藥物動力學不但沒有多少幫助,而且越做越糟。
上面這兩個數據告訴大家:
(1)經過體內系統所發現的抗體的藥物動力學是無可比擬的。體內系統所發現的抗體經過了免疫系統的正向選擇和負向選擇,抗原識別的專一性以及抗體的理化特性都是最好的。相比而言,用體外合成抗體文庫所發現的抗體或多或少會存在抗原識別的多特異性問題,在抗體的理化特性上也不盡如人意。
(2)抗體的工程化改造。如果抗體需要做工程化改造的話,那就請最專業的團隊用最專業的技術,結合抗體工程和蛋白結構、分子模擬來優化抗體的親和力、穩定性和理化特性。
結合以上兩點,您再仔細想一想抗體發現,如果想得到成藥性最好的抗體并且盡可能的避免體外工程化改造,那目前最好的技術平臺就是人源化抗體鼠。
RenMab鼠這座礦脫穎而出
眾多人源化小鼠礦中,RenMabTM小鼠從本專業挖礦磚家的眼中脫穎而出。那就讓磚家從抗體發現角度為大家解讀一下RenMabTM小鼠這座礦與其他人源化小鼠礦相比究竟有什么獨特之處?
經過一番仔細調查研究(某些制藥公司的ZL讀起來真讓人頭疼),磚家總結了以下幾點:
(1) 人源化抗體鼠的構建方式不同。
百奧賽圖用自有知識產權的技術進行了原位替換,用人的整個抗體基因區全面替換了鼠的抗體基因區。再生元的Velocimmune鼠也使用了原位替換的方式,不同的是再生元做的是基于細菌假染色體的多個片段并且多個進程的同源重組。同源重組的構建方式導致了一些抗體多變區或者是調控元件的失活(McDonald L.E. et al, 2014 PNAS; Murphy A.J. et al, 2014 PNAS)。同樣的失活在其它人源化抗體鼠比如Kymab鼠中也被觀測到(Lee E.C., 2014 Nat. Biotechol)。原位替換的方式確保了人源化抗體鼠的免疫應答和野生鼠相似。相對于原位替換,其它的方式包括原位敲除鼠基因再插入人基因或者是敲除/失活鼠基因再異位插入人基因(Trianni鼠,Xenomouse鼠等等),這都或多或少影響了轉基因小鼠的正常免疫應答,比較有名的例子是AlivaMab鼠。
(2) 全區段原位替換最大程度地保證了抗體生成的多樣性。
前面提到的敲除再插入的方式不可避免地會限制V區的選擇,在某個可變區基因有多個拷貝或者突變型的情況下,只能選有代表性的V基因插入。多片段、多進程的方式會造成一些V基因的失活。原位敲除再異位插入會失去天然的抗體V(D)J重組的調控機制。RenMabTM鼠的整個V區應該是所有的抗體人源化鼠中最天然的最接近于人的,人天然抗體基因的拷貝數、內在的各V區之間的原生調控序列以及各種突變型都被最大限度地保持。RenMabTM鼠全區段原位替換的構建方式保證了RenMabTM鼠正常的與野生鼠相似的免疫應答和抗體生成的多樣性。
有看官會問,我明白你在說什么,那小鼠的抗體V(D)J重組機制和人的原生調控序列兼容嗎?這是個非常出色的問題,也是學術界孜孜以求的一個研究方向。在解讀RenMabTM鼠的抗體V(D)J重組機制和人的原生調控序列兼容之前,咱們先看看RenMabTM鼠發育正常嗎?